Uma gota de água
Introdução
A água é a substância mais comum à superfície da Terra. Sem água, a vida não poderia existir. O teu corpo é composto por cerca de 70% de água. Observa a imagem seguinte - A água pode existir em 3 estados:
- Sólido (gelo)
- Líquido (água) e
- Gasoso (vapor de água)
Podes alterar o seu estado através do aquecimento ou do arrefecimento (ou através da alteração da pressão)
Como muda o estado da água?
Quando o gelo é aquecido suavemente, começa a derreter-se e transforma-se em líquido. Se continuares a aquecer, por volta dos 100° Celsius, transforma-se num gás.
Por que razão isto acontece?
A água é uma molécula com a fórmula química H2O, ou seja, dois átomos de hidrogénio ligados a um átomo de oxigénio.
As partículas do gelo sólido são compactas e unidas por ligações químicas chamadas ligações de hidrogénio. Estas estão sempre a vibrar. Quando aqueces o gelo, a energia utilizada aumenta as vibrações. Algumas ligações rompem-se e as partículas ficam livres para se moverem um pouco, é aqui que o gelo se transforma em líquido. À medida que aplicas mais calor, as partículas obtêm energia suficiente para romper todas as ligações e escapar sob a forma de gás ou vapor.
A propriedade física da áqua

A propriedade física da matéria que descreve a ligação estreita entre as partículas individuais da substância chama-se Densidade. A Densidade (D) é a medida da quantidade de matéria (massa ou m) num determinado espaço (volume ou V), expressa como um rácio:
D = m/V.
É a diferença nas densidades da matéria da Terra que provoca as correntes oceânicas, o vento e as placas tectónicas. Geralmente, a densidade da matéria aumenta à medida que passa do estado gasoso para o líquido e, novamente, à medida que passa do estado líquido para o sólido. A densidade também aumenta à medida que a temperatura diminui, porque a descida de temperatura provoca menor vibração dos átomos. Como os átomos não se movem tanto, ficam mais compactados ou densamente unidos. No entanto, a água é diferente!
A água tem algumas propriedades químicas e físicas raras que a tornam numa das mais importantes substâncias do nosso planeta.
Observa o vídeo em que o astronauta da ESA, Frank De Winne, realiza algumas demonstrações para mostrar o comportamento da água em condições de ausência de gravidade na Estação Espacial Internacional. Os professores podem utilizar este vídeo juntamente com os apontamentos abaixo para que as crianças possam comparar o comportamento da água na Terra e no Espaço.
1. Porque é escassa a água sólida (gelo)?
Espera-se que uma substância sólida como o gelo afunde. No entanto, quando colocas uns cubos de gelo numa bebida, o gelo flutua. Enche uma garrafa de plástico com água e rolha-a. Coloca-a no congelador e verifica o que acontece no dia seguinte. Verás que a rolha pode saltar e a garrafa de água parece que se expandiu.
A forma sólida da água (gelo) é MENOS densa do que a forma líquida. A densidade da água pura a quatro graus Celsius é 1,0 g/cm cúbicos, enquanto a densidade do gelo a zero graus Celsius é apenas 0,92 g/cm cúbicos. A água líquida e o gelo têm diferentes densidades, porque, no gelo, as moléculas estão mais afastadas, preenchendo mais espaço do que numa molécula de água líquida.
No espaço: Frank pega num pequeno pedaço de gelo e coloca-o no interior de uma gota de água. O que acontece ao gelo no interior da gota de água? Flutua, afunda-se ou faz outra coisa qualquer?
Respostas:
Na Estação Espacial Internacional, tudo está em QUEDA LIVRE e, por conseguinte, parece não haver força de GRAVIDADE. A gravidade é o que nos impede de flutuar na Terra. Se atirares um objecto ao ar, este cai sempre no chão. Ai!
Esta atracção na direcção da terra chama-se Força Gravitacional. Por conseguinte, tal como os astronautas (e os objectos que não estejam bem presos!), tudo flutua na ISS. Mesmo a água. O gelo não flutua nem se afunda, move-se simplesmente em torno da gota de água.
2. Polaridade da água
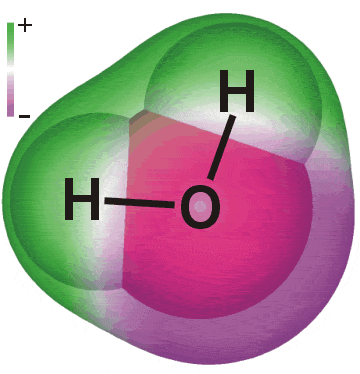
A água é uma molécula bipolar. A fórmula química da água é H2O, ou seja, dois átomos de hidrogénio ligados a um átomo de oxigénio.
Uma molécula de água não tem carga total. Mas existe uma carga ligeiramente negativa na região do átomo de oxigénio e uma carga ligeiramente positiva junto aos átomos de hidrogénio. Chama-se a isto um dipolo. A carga total da molécula da água é nula. As cargas positivas e negativas são iguais, por conseguinte, anulam-se umas às outras.
Experiência: Demonstração da natureza bipolar da água
Materiais:
- Trabalhar numa fonte de água (por ex., uma torneira)
- Uma vareta de vidro ou uma régua de plástico
Método:
- Deixa correr um ligeiro fluxo de água da torneira.
- Pega na régua ou na vareta e aproxima-a do fluxo de água. Acontece alguma coisa?
- Esfrega a régua ou vareta várias vezes numa peça de roupa ou T-shirt. Aproxima-a da água. O que acontece agora? Na tua opinião, por que motivo isto acontece?
Na Estação Espacial Internacional, Frank De Winne utiliza um pedaço de plástico (em vez de uma vareta) para criar alguma carga (ex. carga positiva (+)). Ao esfregar este plástico na roupa, provoca uma acumulação de carga positiva à superfície. Ao aproximar o plástico da gota de água, a carga do plástico atrai a carga oposta das moléculas de água (carga negativa do Oxigénio).
Pergunta de reflexão? Por que motivo Frank não pode ter um fluxo de água na ISS? O que acontece à gota de água quando aproxima o plástico da gota de água?
Resposta:
A vareta ou a régua atrai o fluxo na sua direcção, porque existe uma carga positiva na vareta que atrai a carga negativa da molécula de água.
Quando Frank aproxima o plástico da água, a gota move-se à medida que ele move o plástico carregado. O oxigénio com carga negativa é atraído para a carga positiva do plástico carregado. Frank não pode utilizar um fluxo de água na ISS, porque tudo flutua (está em queda livre) e a água pode entrar facilmente no equipamento eléctrico e provocar danos. A água tem de vir de um saco de água potável especial e necessita de ser absorvida posteriormente.
3. Solubilidade da água

A água possui a propriedade muito importante de ser capaz de dissolver muitos sólidos e gases. O que acontece quando adicionas açúcar (um sólido) ao teu café?
O açúcar é solúvel em água. Algumas coisas são insolúveis (não se dissolvem). Consegues lembrar-te de alguma coisa?
Experiência: O que se dissolve?
Materiais:
cubo de açúcar, pedras de sal, café instantâneo e café moído, pedaços de madeira pequenos (lascas, feno), aparas de plástico pequenas, aparas de velas, garrafas de vidro, colher ou batedora, fonte de água e local para deitar o lixo.
Método:
- Adiciona vários materiais, um de cada vez, numa garrafa com água e observa se a substância se dissolve ou não. Pode ser necessário mexer.
- Faz uma tabela para mostrar os materiais que se dissolvem e os materiais que não se dissolvem.
Na Terra, podemos ver claramente se algo se dissolve, em especial, se tiver cor. Parece “desaparecer” na água. Quando o adicionas ao teu café/chá, este fica doce. (NÃO PROVES NADA na sala de aulas!).
No Espaço, em que as condições são diferentes das da Terra, será que o açúcar também se dissolve no chá? Sabemos que tudo flutua, mas o açúcar flutua na água ou dissolve-se?
Frank tentará dissolver o açúcar neste recipiente de chá. O que pensas que aconteceria se a água estivesse mais quente? Ou fosse mexida?
Os astronautas recebem sacos especiais com chá e açúcar. Necessitam de adicionar água quente e agitar o saco para dissolver o açúcar e misturar o chá. Como é que Frank sabe que o seu chá está doce?
Resposta:
Frank prova o chá e constata que está doce, por conseguinte, o açúcar dissolve-se em água no Espaço.




