Ein tropfen Wasser
Einführung
Wasser ist die häufigste Substanz auf der Erdoberfläche. Ohne sie gäbe es kein Leben. Unser Körper besteht zu 70 % aus Wasser. Schau dir das Bild unten an - Wasser kommt in drei Aggregatzuständen vor:
- fest (Eis)
- flüssig (Wasser) und
-
gasförmig (Wasserdampf)
Sein Zustand kann durch Erhitzen oder Kühlen (oder durch Änderung des Drucks) verändert werden.
Wie verändert sich der Aggregatzustand von Wasser?
Wenn Eis leicht erwärmt wird, beginnt es zu schmelzen und wird flüssig. Bei weiterer Erhitzung wird es bei etwa 100° Celsius zu Gas.
Wie erklärt sich das?
Wasser ist ein Molekül mit der chemischen Formel H2O - zwei an ein Sauerstoffatom gebundene Wasserstoffatome. Die Partikel im festen Eis sind eng zusammengedrückt und über chemische Bindungen namens Wasserstoffbindungen miteinander verbunden. Sie schwingen pausenlos. Wenn wir das Eis erwärmen, verstärkt die dadurch zugeführte Energie die Schwingungen. Einige der Bindungen brechen auf und die Partikel können sich ein wenig bewegen - das Eis wird flüssig. Bei stärkerer Erhitzung erhalten die Partikel genug Energie, um alle Bindungen zu sprengen und in Form von Gas oder Dampf zu entweichen.
Die physikalische Eigenschaft

Die physikalische Eigenschaft, die beschreibt, wie fest die einzelnen Partikel der Substanz zusammengedrückt sind, heißt Dichte. Die Dichte (D) ist ein Maß der Materialmenge (Masse oder m) in einem gegebenen Raum (Volumen oder V). Sie wird ausgedrückt als das Verhältnis:
D = m/V.
Die Differenz in den Dichten der Erdmaterie ist die Antriebskraft für Meeresströmungen, Winde und Plattentektonik.
Normalerweise vergrößert sich die Dichte der Materie, wenn diese vom gasförmigen in den flüssigen Zustand übergeht und ebenso beim Übergang vom flüssigen in den festen Zustand. Auch mit abnehmender Temperatur nimmt die Dichte zu, da die Atome bei niedrigeren Temperaturen weniger schwingen. Wenn die Atome sich nicht so stark bewegen, rücken sie enger - also dichter - zusammen. Wasser verhält sich jedoch anders!
Wasser hat einige sehr ungewöhnliche physikalische und chemische Eigenschaften, die es zu einer der wichtigsten Substanzen auf unserem Planeten machen.
Sieh dir die Videoaufzeichnung des ESA-Astronauten Frank De Winne an, der demonstriert, wie sich Wasser unter Bedingungen der Schwerelosigkeit auf der Internationalen Raumstation verhält. Mit diesem Clip und den nachfolgenden Unterrichtstexten können Lehrkräfte Kindern den Unterschied zwischen dem Verhalten von Wasser auf der Erde und im Weltraum aufzeigen.
1. Weshalb ist festes Wasser (Eis) ungewöhnlich?
Man würde denken, dass eine feste Substanz wie Eis nicht schwimmt, sondern untergeht. Wie wir aber wissen, schwimmen Eiswürfel in unserem Getränk an der Oberfläche.
Fülle eine Plastikflasche mit Wasser und verschließe sie. Lege sie in das Tiefkühlfach und schaue sie dir am nächsten Tag an. Du wirst sehen, dass der Verschluss vielleicht abgeplatzt ist und die Flasche aussieht, als hätte sie sich ausgedehnt.
Die feste Form von Wasser (Eis) ist WENIGER dicht als die flüssige Form. Die Dichte reinen Wassers bei 4 °C beträgt 1,0 g/kcm (Kubikzentimeter) und die Dichte von Eis bei 0 °C liegt nur bei 0,92 g/kcm. Flüssiges Wasser und Eis haben unterschiedliche Dichten, da die Moleküle in Eis weiter voneinander entfernt sind und mehr Raum in Anspruch nehmen als in flüssigem Wasser.
Im Weltraum: Frank nimmt ein kleines Stück Eis und setzt es in einen Wassertropfen. Was passiert mit dem Eis im Wassertropfen? Schwimmt es, sinkt es oder verhält es sich ganz anders?
Antworten:
Auf der Internationalen Raumstation befindet sich alles im FREIEN FALL. Deshalb scheint keine SCHWERKRAFT zu herrschen. Die Schwerkraft ist der Grund, weshalb wir nicht einfach von der Erde wegschweben. Wenn wir etwas in die Luft werfen, landet es stets wieder auf dem Boden. Autsch!
Diese Kraft, die alles zur Erde hinzieht, wird Gravitationskraft genannt. Auf der ISS schwebt also alles, was nicht niet- und nagelfest ist, genau wie die Astronauten umher. Selbst Wasser. Das Eis sinkt nicht und schwimmt nicht, sondern bewegt sich einfach innerhalb des Wassertropfens von einer Stelle zur andern.
2. Polarität von Wasser
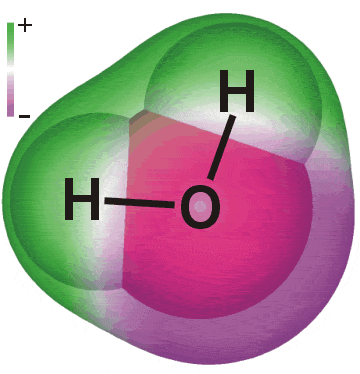
Wassermoleküle sind Dipole. Die chemische Formel für Wasser lautet H2O, - das sind zwei an ein Sauerstoffatom gebundene Wasserstoffatome.
Ein Wassermolekül besitzt keine Gesamtladung. Es besteht jedoch eine geringfügige negative Ladung im Bereich des Sauerstoffatoms und eine geringfügige positive Ladung in der Nähe der Wasserstoffatome. Dies nennt man einen Dipol. Die Gesamtladung des Wassermoleküls ist Null. Die positiven und negativen Ladungen sind gleich groß und heben sich deshalb gegenseitig auf.
Zum Ausprobieren: Veranschaulichung der Dipolarität von Wasser.
Material:
- Arbeite in der Nähe einer Wasserquelle (z. B. Wasserhahn)
- Ein Glasstab oder Kunststofflineal
Durchführung:
- Öffne den Wasserhahn, sodass ein leichter Strahl heraus fließt.
- Halte das Lineal beziehungsweise den Glasstab nahe an den Wasserstrahl. Passiert dabei irgendetwas?
- Reibe nun das Lineal oder den Stab mehrmals mit einem Tuch oder T-Shirt. Halte es wieder nahe an das Wasser. Was geschieht jetzt? Wie erklärst du dir das?
Frank De Winne auf der Internationalen Raumstation verwendet ein Stück Plastik (anstelle eines Stabs), um Ladung zu erzeugen (z. B. positive Ladung +). Dadurch, dass er diesen Kunststoff auf seiner Kleidung reibt, entsteht positive Ladung auf der Oberfläche. Wenn er das Plastikstück nahe an den Wassertropfen hält, zieht die Ladung auf dessen Oberfläche die entgegengesetzte Ladung in den Wassermolekülen an (die negative Ladung des Sauerstoffs).
Denkaufgabe?
Weshalb kann Frank auf der ISS nicht mit einem Wasserstrahl arbeiten? Was passiert mit dem Wassertropfen, wenn er das Plastikstück nahe daran hält?
Antwort:
Der Stab beziehungsweise das Lineal ziehen den Wasserstrahl an, da eine positive Ladung auf ihrer Oberfläche die negative Ladung im Wassermolekül anzieht. Wenn Frank das Plastikstück nahe an das Wasser hält und es bewegt, müsste sich der Tropfen ebenso bewegen. Der negativ geladene Sauerstoff wird von der positiven Ladung des aufgeladenen Kunststoffs angezogen.
Frank kann auf der ISS keinen Wasserstrahl verwenden, da alles schwebt (alles befindet sich im freien Fall) und das Wasser leicht in elektrische Geräte eindringen und Schäden verursachen kann. Er muss Wasser aus einem speziellen Trinkwasserbeutel verwenden, das anschließend aufgewischt werden muss.
3. Wasserlöslichkeit:

Wasser besitzt die sehr wichtige Eigenschaft, viele Feststoffe und Gase lösen zu können. Was geschieht, wenn du Zucker (einen Feststoff) in Kaffee gibst?
Zucker wird als wasserlöslich bezeichnet. Einige Dinge sind unlöslich (sie lösen sich nicht auf). Fallen dir Beispiele ein?
Zum Ausprobieren: Was ist löslich?
Material:
Würfelzucker, Salzkörner, Instantkaffee und Kaffeesatz, kleine Holzstückchen (Späne, Heu), kleine Kunststoffspäne, Kerzenspäne, Einmachgläser, Löffel oder Rührer, Wasserquelle und einen Platz für den Abfall.
Durchführung;
- Gib die unterschiedlichen Materialien einzeln in ein Glas mit Wasser und beobachte, ob sie sich lösen oder nicht. Möglicherweise musst du umrühren.
- Erstelle eine Tabelle, in der du vermerkst, was sich löst und was nicht.
Auf der Erde können wir leicht erkennen, ob ein Material löslich ist. Besonders dann, wenn das Material eine Farbe hat. Es scheint dann im Wasser zu „verschwinden“. Unser Tee oder Kaffee schmeckt dadurch süß. (IM KLASSENZIMMER NICHTS KOSTEN!)
Im Weltraum herrschen andere Bedingungen als auf der Erde. Würde sich der Zucker dort auch im Tee lösen? Wie wir wissen, schwebt alles umher. Aber würde der Zucker auch nur einfach im Wasser umher schwimmen oder sich tatsächlich auflösen?
Frank versucht nun, Zucker in seinem Teebehälter zu lösen. Was würde deiner Meinung nach geschehen, wenn das Wasser wärmer wäre? Oder wenn er es umrühren würde?
Astronauten erhalten spezielle Beutel mit Tee und Zucker. Sie müssen warmes Wasser hinzufügen und den Beutel schütteln, um den Zucker zu lösen und den Tee zusammenzumischen. Woher weiß Frank, ob sein Tee süß ist?
Antwort:
Frank probiert seinen Tee und er schmeckt süß. Also löst sich Zucker auch im Weltraum in Wasser.




