Pisara vettä
Johdanto
Vesi on yleisin aine Maan pinnalla. Ilman sitä elämää ei voisi olla olemassa. Ihmisen kehosta 70 % on vettä. Katso alla olevaa kuvaa − vedellä voi olla kolme erilaista olomuotoa:
- kiinteä aine (jää)
- neste (vesi) ja
- kaasu (vesihöyry).
Veden olomuotoa voidaan muuttaa kuumentamalla tai jäähdyttämällä sitä (tai muuttamalla painetta).
Miten veden olomuoto muuttuu?
Kun jäätä lämmitetään varovasti, se alkaa sulaa ja muuttuu nestemäiseksi. Kun sitä lämmitetään edelleen noin 100 °C:seen, se muuttuu kaasuksi.
Miksi näin käy?
Vesi on molekyyli, jonka kemiallinen kaava on H2O: kaksi vetyatomia yhteen happiatomiin sitoutuneina. Kiinteän jään sisältämät hiukkaset ovat pakkautuneet tiiviisti yhteen ja yhdistyneet kemiallisilla sidoksilla, joita sanotaan vetysidoksiksi. Ne värähtelevät koko ajan. Kun jäätä kuumennetaan, siihen kohdistuva energia lisää tätä värähtelyä. Jotkin sidoksista purkautuvat, ja hiukkaset pääsevät liikkumaan jonkin verran − tällöin jää muuttuu nestemäiseksi. Kun hiukkasiin kohdistetaan lisää lämpöä, ne saavat riittävästi energiaa purkaakseen kaikki sidoksensa ja vapautuakseen kaasuna tai höyrynä.
Veden fysikaaliset ominaisuudet

Aineen fysikaalista ominaisuutta, joka kuvaa sitä, miten tiiviisti sen yksittäiset hiukkaset ovat pakkautuneet, sanotaan tiheydeksi. Tiheys (D) on materiaalin määrän (massan eli m) yksikkö tietyssä tilassa (tilavuudessa eli V), ja se ilmaistaan näiden suhteena:
D = m/V.
Juuri Maan aineiden välinen tiheysero saa aikaan merivirrat, tuulen ja mannerlaattojen liikkeet.
Yleensä aineen tiheys kasvaa sen muuttuessa kaasusta nesteeksi ja vastaavasti nesteestä kiinteäksi aineeksi. Lisäksi tiheys kasvaa lämpötilan aletessa, koska lämpötilan aleneminen vähentää atomien värähtelyä. Kun atomit liikkuvat vähemmän, ne pakkautuvat tiiviisti toistensa lähelle. Mutta vesi on erilaista!
Vedellä on joitakin hyvin epätavallisia fysikaalisia ja kemiallisia ominaisuuksia, joiden vuoksi se on yksi tärkeimmistä aineista planeetallamme.
Katso video, jossa ESAn astronautti Frank De Winne esittää, miten vesi käyttäytyy painottomissa olosuhteissa kansainvälisellä avaruusasemalla. Opettajat voivat käyttää videon tätä osaa yhdessä tekstiosan kanssa, jotta nuoremmat oppilaat voivat verrata, miten vesi käyttäytyy Maassa ja avaruudessa.
1. Miksi kiinteä vesi (jää) on poikkeuksellista?
Odottaisit ehkä, että jään kaltainen kiinteä aine uppoaa. Olet kuitenkin huomannut, että juotavaan nesteeseen laitetut jääpalat jäävät kellumaan.
Täytä muovipullo vedellä ja sulje korkki. Laita pullo pakastimeen ja tarkista, miltä se näyttää seuraavana päivänä. Huomaat, että korkki saattaa ponnahtaa pois ja vesipullo näyttää ikään kuin laajentuneelta.
Veden kiinteä muoto (jää) on VÄHEMMÄN tiivistä kuin sen nestemäinen muoto. Puhtaan veden tiheys neljässä celsiusasteessa on 1,0 g/cm², kun jään tiheys puolestaan nollassa celsiusasteessa on vain 0,92 g/cm². Nestemäisen veden ja jään tiheydet ovat erilaiset, koska jäässä molekyylit ovat kaukana toisistaan vieden enemmän tilaa kuin nestemäisessä vedessä oleva molekyyli.
Avaruudessa: Frank ottaa pienen jääpalan ja laittaa sen vesikuplan sisään. Mitä jäälle tapahtuu vesikuplan sisällä? Kelluuko se vai uppoaako se vai tapahtuuko sille jotain muuta?
Vastaukset:
Kansainvälisellä avaruusasemalla kaikki on VAPAAN PUDOTUKSEN tilassa, joten siellä ei näyttäisi olevan PAINOVOIMAA. Juuri painovoiman ansiosta emme leiju pois maapallolta. Jos heität jotain ilmaan, se laskeutuu aina takaisin maahan. Auts!
Voimaa, joka vetää kaikkia kappaleita Maata kohti, sanotaan painovoimaksi. Aivan samalla tavalla kuin astronautit (ja mikä tahansa, jota ei ole kiinnitetty tiukasti), kaikki leijuu ISS-asemalla. Myös vesi. Jää ei kellu eikä uppoa, vaan se yksinkertaisesti liikkuu ympäriinsä vesikuplan sisällä.
2. Veden polaarisuus
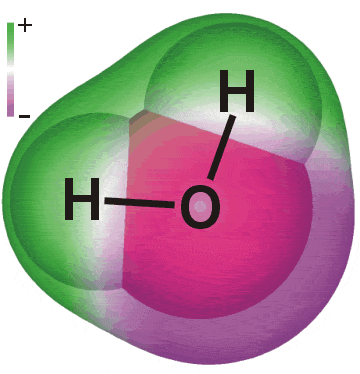
Vesi on dipolaarinen molekyyli. Veden kemiallinen kaava on H2O: kaksi vetyatomia yhteen happiatomiin sitoutuneina.
Vesimolekyylillä ei ole kokonaisvarausta. Happiatomin alueella on kuitenkin pieni negatiivinen varaus ja vetyatomien lähellä pieni positiivinen varaus. Tätä sanotaan dipoliksi. Vesimolekyylin kokonaisvaraus on nolla. Koska positiiviset ja negatiiviset varaukset ovat yhtä suuret, ne eivät voi kumota toisiaan.
Koe: veden dipolisen luonteen osoittaminen
Tarvikkeet:
- vesilähde (esimerkiksi vesihana)
- lasitanko tai muovinen viivoitin
Toimenpiteet:
- Laske hanasta vettä pienellä paineella.
- Laita viivoitin tai tanko vesivirran lähelle. Tapahtuuko mitään?
- Hankaa nyt viivoitinta tai tankoa useita kertoja kankaaseen tai T-paitaan. Vie se veden lähelle. Mitä nyt tapahtuu? Miksi arvelet näin tapahtuvan?
Kansainvälisellä avaruusasemalla Frank De Winne synnyttää pienen varauksen (esimerkiksi positiivisen (+) varauksen) muovipalan avulla (tangon sijasta). Hankaamalla tätä muovia vaatteisiinsa hän saa aikaan positiivisen varauksen syntymisen pintaan. Kun muovi tuodaan lähemmäksi vesipisaraa, sen varaus vetää puoleensa vesimolekyylien vastakkaista varausta (hapen negatiivista varausta).
Pohdittavia kysymyksiä:
Miksi Frank ei voi käyttää vesivirtaa ISS-asemalla? Mitä vesikuplalle tapahtuu, kun hän vie muovin lähemmäksi sitä?
Vastaus:
Tanko tai viivoitin vetää virtaa puoleensa, koska tangossa on positiivinen varaus, joka vetää puoleensa vesimolekyylin negatiivista varausta.
Kun Frank vie muovin veden lähelle, pisaran pitäisi liikkua ympäriinsä samalla, kun hän liikuttaa varautunutta muovia ympäriinsä. Varautuneen muovin positiivinen varaus vetää puoleensa negatiivisesti varautunutta happea.
Frank ei voi käyttää vesivirtaa ISS-asemalla, koska kaikki leijuu (on vapaan pudotuksen tilassa), ja vesi voisi päästä helposti sähkölaitteisiin aiheuttaen vahinkoja. Vesi on otettava erityisestä juomavesipussista, ja roiskeet on sen jälkeen kuivattava pois.
3. Veden liukenevuus

Eräs veden tärkeä ominaisuus on sen kyky liuottaa monia kiinteitä aineita ja kaasuja. Mitä tapahtuu, kun lisäät sokeria (kiinteää ainetta) kahviisi?
Sokerin sanotaan olevan veteen liukeneva. Jotkin aineet ovat liukenemattomia (eivät liukene). Osaatko mainita joitakin sellaisia aineita?
Koe: mikä liukenee?
Tarvikkeet:
sokeripala, suolarakeita, pikakahvia ja kahvijauhoja, pieniä puunpalasia (lastuja, sahanpuruja), pieniä muovisiruja, kynttilän lastuja, lasipurkkeja, lusikka tai vispilä, vesilähde ja jäteastia.
Toimenpiteet:
- Lisää erilaiset aineet yksi kerrallaan purkissa olevaan veteen ja seuraa, liukeneeko aine. Joudut mahdollisesti sekoittamaan nestettä.
- Laadi taulukko ja merkitse siihen, mikä aineista liukenee ja mikä ei.
Maassa näemme selvästi, jos jokin aine liukenee, varsinkin, jos aine on värillistä. Se näyttää ”katoavan” veden sekaan. Kun lisäämme sitä teehen tai kahviin, se maistuu makealta. (ÄLÄ MAISTA MITÄÄN tunnilla!)
Liukenisiko sokeri teehen avaruudessa, jossa olosuhteet ovat erilaiset kuin maassa? Tiedämme, että kaikki leijuu, mutta kävisikö niin, että sokeri ainoastaan leijuisi ympäriinsä vedessä vai sulaisiko se todellakin?
Frank yrittää liuottaa sokeria teekuppiinsa. Mitä arvelet tapahtuvan, jos vesi olisi lämpimämpää? Tai jos juomaa sekoitettaisiin? Astronauteilla on teetä ja sokeria sisältäviä erikoispusseja. He lisäävät kuumaa vettä ja ravistavat pussia, jotta sokeri liukenee ja sekoittuu teehen. Mistä Frank tietää, milloin hänen teensä on makeaa?
Vastaus:
Maistaessaan teetä Frank huomaa sen olevan makeaa, joten sokeri todellakin liukenee veteen avaruudessa.




