Kapka vody
Úvod
Voda je nejběžnější látkou na povrchu Země. Bez ní by život nemohl existovat. Vaše tělo je asi ze 70 % tvořeno vodou. Podívejte se na následující obrázek - voda může existovat ve 3 skupenstvích:
- pevném (led),
- kapalném (voda) a
-
plynném (vodní pára).
Skupenství vody lze měnit zahřátím nebo ochlazením (nebo změnou tlaku).
Jak se mění skupenství vody?
Když se led mírně zahřeje, začne tát a mění se na kapalinu. Pokud v zahřívání pokračujete, asi při 100 °C se změní na plyn.
Proč se to stane?
Voda je molekula, která má chemický vzorec2O, a má tedy dva atomy vodíku navázané na jeden atom kyslíku. Částice v pevném skupenství, ledu, jsou uloženy těsně u sebe a spojeny chemickými vazbami, které se nazývají vodíkové můstky. Neustále vibrují. Když led zahřejete, vložená energie vibrace zvětší. Některé z vazeb se poruší, částice se uvolní a mohou se tak trochu pohybovat - v tomto okamžiku se z ledu stává kapalina. Se zvýšením přísunu tepla získají částice dostatečnou energii na rozložení všech vazeb a unikají ve formě plynu (páry).

Fyzikální vlastnost hmoty, která popisuje, jak těsně jsou částice v látce uspořádané, se nazývá hustota. Hustota (D) je měřítkem množství materiálu (hmotnost neboli m) v daném prostoru (objem neboli V) a je vyjádřena poměrem:
D = m/V.
Rozdíly v hustotě zemské hmoty jsou tím, co řídí mořské proudy, vítr a deskovou tektoniku.
Hustota hmoty se obvykle zvyšuje při změně z plynného na kapalné skupenství a znovu při změně z kapalného skupenství na tuhé. Hustota se též zvyšuje při poklesu teploty, neboť pokles teploty způsobuje snížení vibrací atomů. Atomy se tolik nepohybují, a proto je jejich uspořádání těsnější, tj. hustší. Voda je však odlišná! Voda má některé velmi neobvykle fyzikální a chemické vlastnosti, které ji činí jednou z nejdůležitějších látek na naší planetě.
Podívejte se na video s kosmonautem ESA Frankem De Winne, který ukazuje, jak se voda chová ve stavu beztíže na Mezinárodní vesmírné stanici. Pedagogové mohou tento klip použít společně s následujícími poznámkami k lekcím, aby malé děti mohly porovnat chování vody na Zemi a ve vesmíru.
1. Solid water – how unusual is this solid!
Proč se voda v pevném skupenství (led) chová jinak?
Předpokládali byste, že se pevná látka, jako je voda, potopí. Víte však, že když si dáte několik kostek ledu do nápoje, plavou. Naplňte umělohmotnou láhev vodou a zavřete ji. Dejte ji do mrazničky a další den se podívejte, jak vypadá. Uvidíte, že víčko možná odskočilo a láhev vody vypadá, jako by se zvětšila.
Pevná forma vody (led) má NIŽŠÍ hustotu než tekutá forma. Hustota čisté vody při čtyřech stupních Celsia je 1,0 g/cm3, zatímco hustota ledu při nula stupních Celsia je pouze 0,92 g/cm3. Voda v tekutém stavu a led mají různou hustotu, protože v ledu jsou molekuly od sebe více vzdáleny a vyplní tak větší prostor než v molekule tekuté vody.
Ve vesmíru: Frank vezme kousek ledu a vloží jej do kapky vody. Co se stane s ledem v kapce vody? Bude se vznášet, klesne nebo se zachová jinak?
Odpovědi:
Na Mezinárodní vesmírné stanici je vše ve VOLNÉM PÁDU a neměla by tu tedy působit GRAVITACE. Gravitace je síla, která nám brání v tom, abychom se zde na Zemi vznášeli. Když něco hodíte, vždy to dopadne na zem. Au!
Tato tíže přitahující všechno k Zemi se nazývá gravitační síla. Na ISS se proto všechno vznáší stejně jako kosmonauti (a vše, co není pevně připevněno!). I voda. Led se nebude vznášet ani neklesne, ale bude se prostě pohybovat ve vodní kapce.
2. Polarita vody
Voda je bipolární molekula.Voda má chemický vzorec H2O , což jsou dva atomy vodíku navázané na jeden atom kyslíku. Molekula vody nemá žádný celkový náboj. V místě kyslíkového atomu je však slabý záporný náboj a v místě atomů vodíku je slabý kladný náboj. Tento jev se nazývá dipól. Celkový náboj molekuly vody je nulový. Kladné náboje a záporné náboje se vzájemně rovnají, takže se vyruší.
Vyzkoušejte: Demonstrace bipolárního charakteru vody
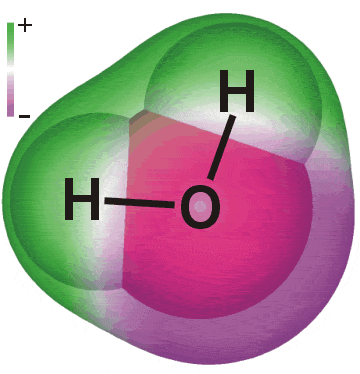
Pomůcky:
- Zdroj vody (například vodovodní kohoutek)
- • Skleněná tyčinka nebo umělohmotné pravítko
Postup:
- Nechte z kohoutku téci malý proud vody.
- Vezměte pravítko nebo tyčinku a přiložte je k proudu vody. Stalo se něco?
- Nyní přetřete pravítko nebo tyčinku několikrát látkou nebo tričkem. Přiložte je do blízkosti vody. Co se děje teď? Proč myslíte, že se to stalo?
Na Mezinárodní vesmírné stanici používá Frank De Winne pro vytvoření náboje (např. kladný náboj +) kousek umělé hmoty (místo tyčinky). Tím, že otře umělou hmotu oděvem, způsobí, že se na jejím povrchu vytvoří kladný náboj. Když přiloží umělou hmotu do blízkosti kapky vody, náboj na umělé hmotě přitáhne opačný náboj na molekule vody (záporný náboj kyslíku).
Thinking question:
Why can’t Frank have a stream of water on the ISS? What happens to the drop of water when he brings the plastic closer to it?
Answer:
The rod or ruler will attract the stream towards it as there is a positive charge on the rod and it will attract the negative charge on the water molecule.
As Frank brings the plastic close to the water the drop should move around as he moves the charged plastic around. The negative charged oxygen will be attracted to the positive charge on the charged plastic.
Frank cannot use a stream of water on the ISS because everything floats (is in free fall) and the water can easily get into electrical equipment and cause damage. The water has to come from a special drinking water bag and needs to be mopped up afterwards.
3. Solubility of water

Water has a very important property of being able to dissolve many solids and gases. What happens when you add sugar (a solid) to your coffee? Sugar is said to be soluble in water. Some things are insoluble (will not dissolve). Can you think of any? Water is clear so when you dissolve something in it, the water can change colour.
To try: What dissolves?
Materials:
sugar cube, salt grains, instant coffee and coffee grounds, small pieces of wood (shavings, hay), small shavings of plastic, candle shavings, glass jars, spoon or stirrer, source of water and place to dispose of the waste.
Method:
- Add one at a time, various materials to water in a jar and see if the substance dissolves or not. You may need to stir.
- Make a table to show what dissolves and what does not.
On Earth, we can see clearly if something dissolves especially if it has a colour. It seems to ‘disappear’ into the water. When we add it to our tea/coffee, it tastes sweet (DO NOT TASTE ANYTHING in the classroom!).
In Space, where the conditions are different than on Earth, would sugar also dissolve in tea? We know everything floats but would the sugar just float around in the water or will it actually dissolve?
Frank will try to dissolve sugar in his tea container. What do you think would happen if the water was warmer? Or stirred? Astronauts get special bags which contain tea and sugar. They need to add warm water and shake the bag to dissolve the sugar and mix the tea together. How will Frank know his tea is sweet?
Answer:
Frank tastes his tea and it is sweet so sugar does actually dissolve in water in space.















 Germany
Germany
 Austria
Austria
 Belgium
Belgium
 Denmark
Denmark
 Spain
Spain
 Estonia
Estonia
 Finland
Finland
 France
France
 Greece
Greece
 Hungary
Hungary
 Ireland
Ireland
 Italy
Italy
 Luxembourg
Luxembourg
 Norway
Norway
 The Netherlands
The Netherlands
 Poland
Poland
 Portugal
Portugal
 Czechia
Czechia
 Romania
Romania
 United Kingdom
United Kingdom
 Slovenia
Slovenia
 Sweden
Sweden
 Switzerland
Switzerland


























